Anvisa autoriza uso emergencial do quarto medicamento contra COVID
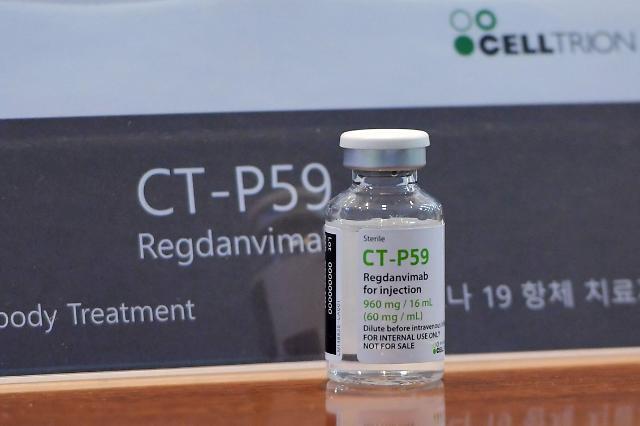
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou ontem, quarta-feira (11), o uso emergencial, em caráter experimental, do medicamento Regdanvimabe, que é o quarto medicamento autorizado no Brasil para tratamento da covid-19. A aprovação foi concedida por unanimidade entre os diretores do órgão. 

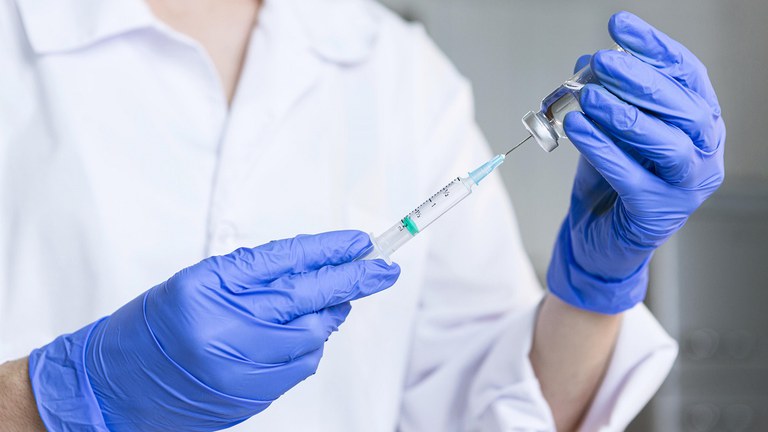
O Regdanvimabe é indicado para o tratamento de covid-19 leve a moderada em pacientes adultos que não necessitem de suplementação de oxigênio, com infecção por Sars-CoV-2 confirmada por laboratório e que apresentem alto risco de progressão para a doença em sua forma mais grave. O medicamento utiliza a tecnologia de anticorpo monoclonal. Trata-se de um produto biológico produzido em laboratórios e que reproduz anticorpos que ajudam o organismo no combate a alguma doença específica.
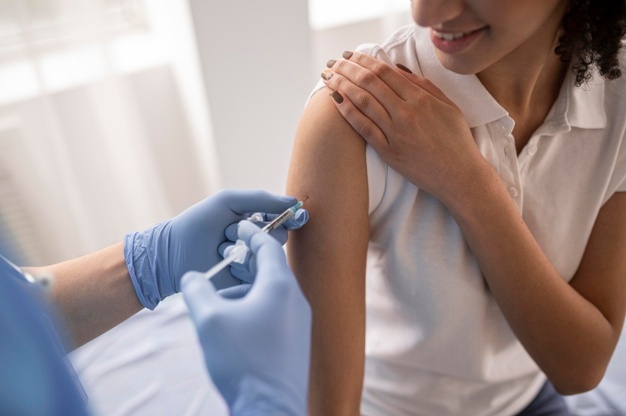
De acordo com a Anvisa, o produto é injetável e de uso restrito a hospitais, preferencialmente para uso em programas de saúde pública no combate ao coronavírus. Ele não poderá ser vendido por farmácias ou drogarias. A dose recomendada é uma única de 40 miligrama por quilo. O medicamento deve ser administrado após teste viral positivo para Sars-CoV-2 e dentro de sete dias após o início dos sintomas.
Entre os grupos de risco citados pela agência reguladora, estão pessoas com obesidade, diabetes, doença renal, idosos, indivíduos acima de 55 anos que tenham doença cardiovascular ou pulmonar crônica, diabetes, doença renal ou hepática crônica e imunossupressão.
O medicamento não está indicado para uso em pacientes que estejam hospitalizados devido a complicações da covid-19 e que necessitem de suporte de oxigênio. No caso das grávidas, segundo a Anvisa, os anticorpos gerados pelo Regdanvimabe são conhecidos por cruzar a barreira placentária e, portanto, teria potencial para ser transferido da mãe para o feto.
“É desconhecido, porém, se essa transferência fornece qualquer benefício ou risco. Tendo em vista o limitado conhecimento sobre o produto, seu uso na gravidez só deve ser considerado se o possível benefício para o paciente for superior a eventuais riscos para o feto”, informou a agência.